Fala editada de diretor da Anvisa sobre “risco grave” de vacinas anticovid volta a circular em 2023
- Este artigo tem mais de três anos.
- Publicado em 29 de março de 2023 às 15:21
- 4 minutos de leitura
- Por AFP Brasil
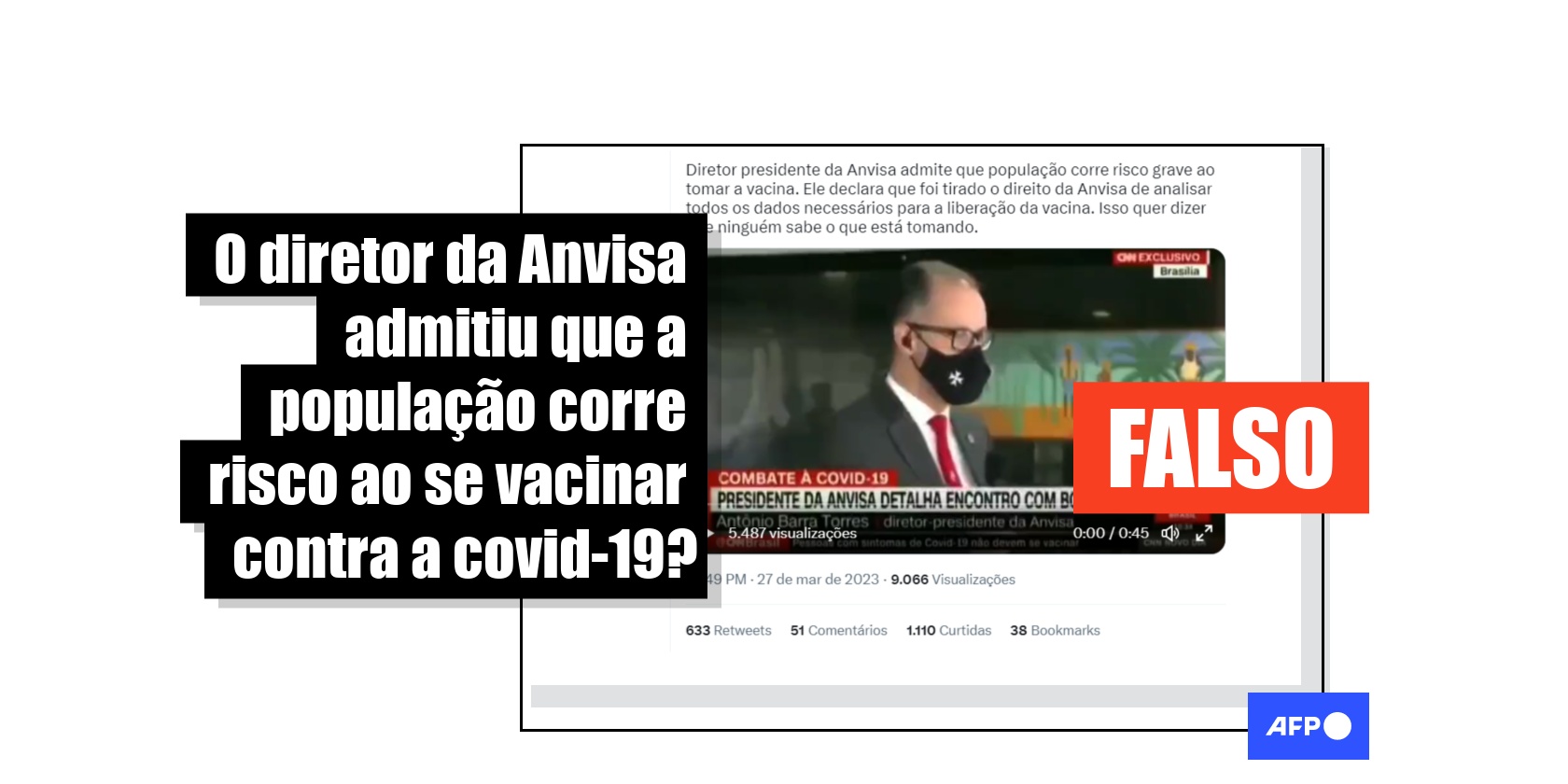
“Diretor presidente da Anvisa admite que população corre risco grave ao tomar a vacina. Ele declara que foi tirado o direito da Anvisa de analisar todos os dados necessários para a liberação da vacina. Isso quer dizer que ninguém sabe o que está tomando”, afirma um usuário que compartilhou o conteúdo no Twitter em março de 2023.
No Facebook, um usuário compartilhou a sequência, questionando: “E ai, já tomou a 5ª dose?”.
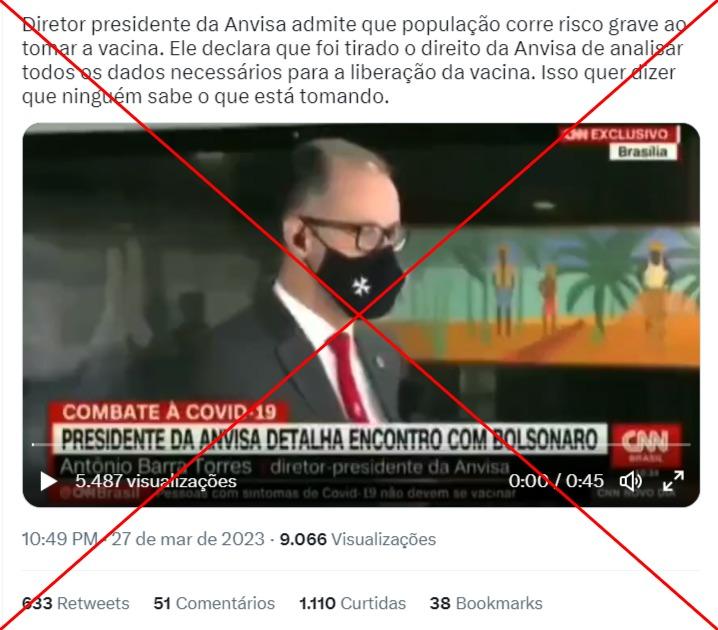
O vídeo viralizado contém trechos de uma entrevista do diretor-presidente da Anvisa, Antonio Barra Torres, à CNN Brasil, em que ele fala sobre um “risco sanitário grave”, respondendo a uma pergunta sobre perigos para a população.
A sequência circula em 2023 em meio à aplicação de vacinas bivalentes da Pfizer no país, que receberam a aprovação da Anvisa para uso emergencial em novembro de 2022. O objetivo dos imunizantes é, além de proteger contra a cepa original do coronavírus, oferecer proteção também contra a variante ômicron.
A fala do presidente da Anvisa, porém, não tem relação com os imunizantes bivalentes e tampouco com as versões monovalentes das vacinas.
Entrevista à CNN Brasil em 2021
Uma pesquisa no Google pelos termos “Antonio Torres risco sanitário grave CNN” localizou a entrevista original, concedida em 10 de fevereiro de 2021 à emissora, e que tinha como contexto uma medida provisória que buscava acelerar o processo de aquisição de vacinas contra a covid-19.
A entrevista completa mostra que Barra Tores referia-se ao artigo 5º, agregado à Medida Provisória 1.003/2020, que faria com que a agência não mais analisasse os pedidos de farmacêuticas, devendo “conceder autorização” às solicitações que tivessem sido aprovadas por agências reguladoras de outros países, em um prazo de até cinco dias.
Após cerca de dois minutos do vídeo da entrevista publicado pela CNN Brasil, a analista de política Basília Rodrigues pergunta a Barra Torres, em um trecho que não aparece na sequência viral: “Por que o senhor tem essa avaliação, de que a medida provisória tira, então, essa competência de análise da Anvisa? O senhor explicou isso para o presidente?”.
Em resposta, o diretor da agência regulatória profere um dos trechos usados no conteúdo viralizado: “Está escrito no artigo 5º, logo na primeira sentença, lá diz: A Anvisa concederá autorização, então não há margem a mais nada. A Anvisa seria reduzida a uma atividade cartorial, uma atividade de conferência de documentos, um checklist, sem nenhuma análise de mérito”.
Aproximadamente aos sete minutos da entrevista, a jornalista Luciana Barreto pergunta: “O risco desse artigo 5º que o senhor falou agora, e da retirada de autonomia da Anvisa, na prática, para a população, a gente corre algum risco?”. No conteúdo viral, a primeira parte dessa pergunta, que faz referência ao artigo 5º da Medida Provisória e à retirada de autonomia da Anvisa, foi omitida.
“Corre risco sanitário grave”, respondeu o presidente da Anvisa, sobre a impossibilidade de análise de pedidos pela agência reguladora. “Simples assim. Porque o fato de estar aprovado/registrado em outro país não necessariamente autoriza o uso no Brasil sem riscos. E é fácil de entender: nós temos uma série de verificações a serem feitas”, disse Barra Torres.
O posicionamento de Barra Torres, portanto, não se referia à segurança das vacinas, e sim “à possibilidade, caso aprovada uma Medida Provisória proposta pelo Congresso, de liberação rápida de vacinas sem a análise técnica da Anvisa”, explicou a agência reguladora ao AFP Checamos em 14 de janeiro de 2022.
“O diretor-presidente referia-se a um cenário hipotético, que ao fim e ao cabo, e com final feliz para a população brasileira, acabou não se realizando. Todas as vacinas à disposição no Brasil, e até hoje aprovadas para uso pela população, passaram pela análise técnica da agência, com total garantia pelo órgão de que possuem segurança, qualidade e eficácia”, completou a Anvisa na data.
Veto
O artigo 5º foi vetado pelo então presidente Jair Bolsonaro (2019-2022), por, entre outras razões, contrariar o interesse público “ao tornar compulsória a autorização temporária de uso emergencial para a importação, de forma a dispensar a prévia análise técnica por parte da Anvisa acerca da segurança, qualidade e eficácia em cada caso”.
Com 37 dispositivos vetados no total, a Lei 14.121/2021 está em vigor.
Em 17 de março de 2023, a Anvisa divulgou uma nota a respeito da ampliação do prazo de validade das vacinas bivalentes na qual reforçou que “as vacinas continuam sendo essenciais no combate à covid-19, especialmente na prevenção de casos graves e mortes”.
Referências
- Nota da Anvisa sobre aprovação de vacinas bivalentes
- Entrevista de Antonio Barra Torres à CNN Brasil
- Entrevista de Antonio Barra Torres no canal da CNN Brasil no YouTube
- Quadro Comparativo do Senado sobre a MP nº 1003/2020
- Vetos à MP nº 1003/2020
- Justificativa dos vetos à MP nº 1003/2020
- Texto atual da Lei nº 14.121 de 01/03/2021
- Nota da Anvisa sobre vacinas bivalentes
Copyright © AFP 2017-2026. Qualquer uso comercial deste conteúdo requer uma assinatura. Clique aqui para saber mais.