Postagens enganosas sobre os “riscos” de cada vacina contra covid-19 não consideram os benefícios
- Este artigo tem mais de quatro anos.
- Publicado em 11 de agosto de 2021 às 23:08
- Atualizado em 15 de janeiro de 2026 às 20:26
- 9 minutos de leitura
- Por AFP Brasil
Publicações que apontam os supostos riscos de quatro vacinas contra a covid-19 somam mais de 12.000 interações nas redes sociais desde julho de 2021. Embora efeitos adversos tenham sido relatados, sua ocorrência é considerada rara para todos os imunizantes citados nas publicações - Janssen, Pfizer, AstraZeneca e CoronaVac. As vacinas contra a covid-19 utilizadas no Brasil são monitoradas pela Anvisa, que mantém a recomendação de continuidade da vacinação por considerar que, até o momento, os benefícios superam os riscos.
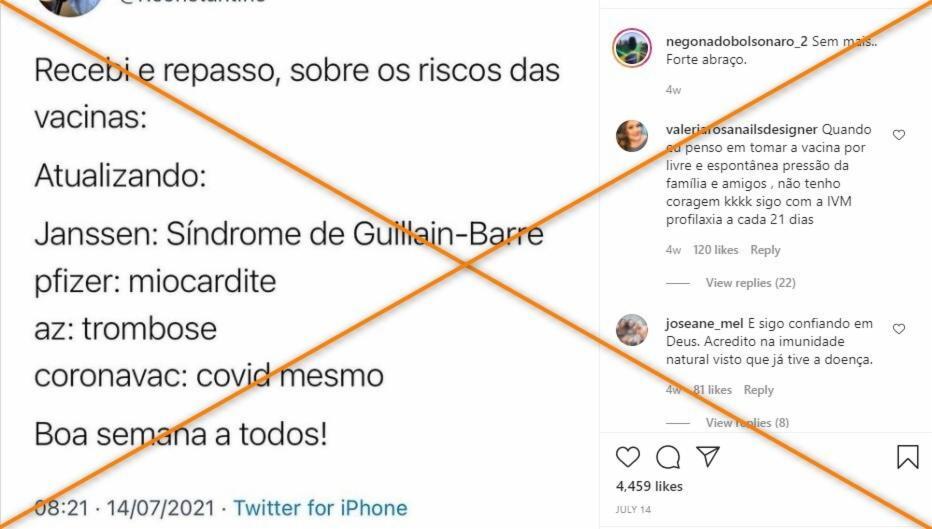
“Recebi e repasso, sobre os riscos das vacinas: Atualizando: Janssen: Síndrome de Guillain-Barre pfizer: miocardite az: trombose coronavac: covid mesmo”, diz uma postagem no Facebook (1, 2). O mesmo conteúdo também circulou no Instagram (1, 2) e no Twitter (1).
Janssen e a Síndrome de Guillain-Barré (SGB)
Segundo o Ministério da Saúde, a Síndrome de Guillain-Barré (SGB) é uma doença rara que causa um distúrbio autoimune com impactos no sistema nervoso. “Geralmente provocada por um processo infeccioso anterior, manifesta fraqueza muscular, com redução ou ausência de reflexos”, diz a pasta.
A Agência Nacional de Vigilância Sanitária (Anvisa) explica que “episódios pós-vacinação (eventos adversos) [relacionados à SGB] também são raros, mas já conhecidos e relacionados a outras vacinas, como a da influenza (gripe)”.
Em 13 de julho de 2021, a Agência de Medicamentos e Alimentos (FDA) dos Estados Unidos anunciou que atualizaria a ficha técnica da vacina Janssen contra a covid-19, desenvolvida pelo grupo Johnson & Johnson, para incluir informações relativas a um “maior risco observado de SGB após a vacinação”.
Na data do anúncio, a agência norte-americana reportou 100 notificações preliminares de SGB após a vacinação com a Janssen, em um contexto de aproximadamente 12,5 milhões de doses administradas. Dessas notificações, 95 eram graves e exigiram hospitalização. Houve uma morte relatada. “A cada ano, nos Estados Unidos, cerca de 3.000 a 6.000 pessoas desenvolvem SGB”, assinalou a FDA.
Uma consulta feita em 11 de agosto de 2021 na plataforma Notificação de Eventos Adversos à Vacina (Vaers) dos Estados Unidos mostrou 118 eventos descritos como casos da Síndrome de Guillain-Barré relacionados à vacina da Janssen.
A plataforma, no entanto, explica que as notificações ali contidas, por si só, não podem ser usadas para determinar se uma vacina causou ou contribuiu para um evento adverso ou uma doença em específico: “Em sua maior parte, as notificações contidas na Vaers são voluntárias, o que significa que são sujeitas a vieses”. Até 10 de agosto de 2021, já haviam sido aplicadas mais de 13,7 milhões de doses do imunizante nos EUA, de acordo com os Centros para o Controle e Prevenção de Doenças (CDC).
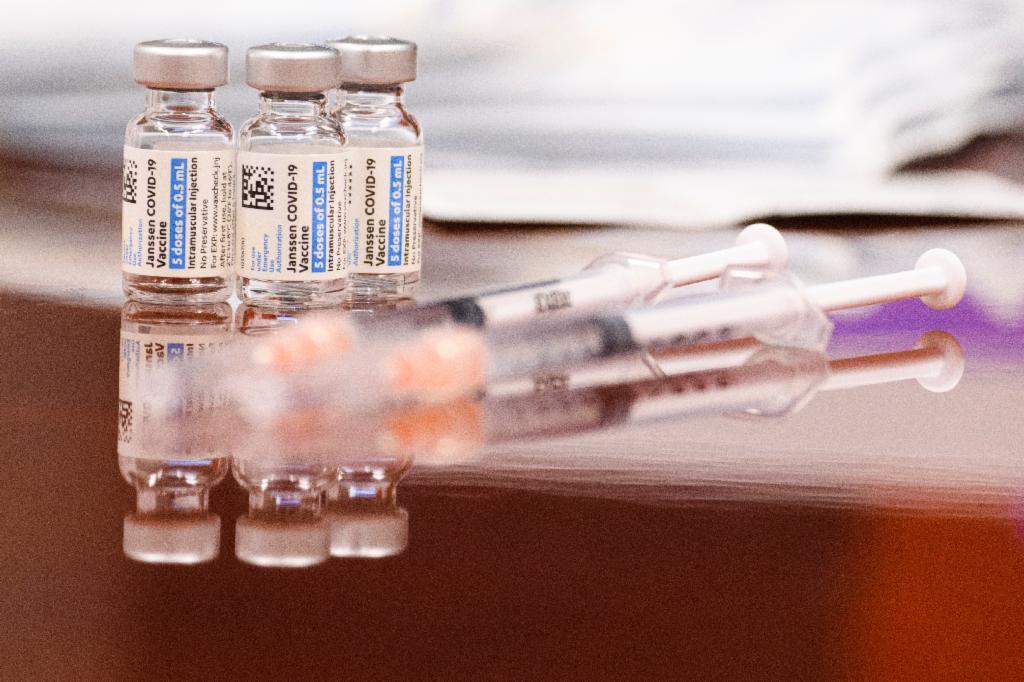
Em julho de 2021, o grupo Johnson & Johnson emitiu uma nota, afirmando que casos raros da doença neurológica foram relatados após o uso da vacina Janssen. A maioria ocorreu dentro de 42 dias após a vacinação. “Embora a chance de isso ocorrer seja muito baixa, a Johnson & Johnson atualizou sua ficha técnica da vacina da covid-19 para incluir informações importantes sobre esses casos raros e sobre os sinais e sintomas da síndrome de Guillain-Barré”, disse a empresa, em tradução livre do inglês.
No Brasil, a Anvisa fez um comunicado em 26 de julho de 2021 sobre casos raros de Síndrome de Guillain-Barré após a imunização contra a covid-19 com as vacinas AstraZeneca/Fiocruz, Janssen e CoronaVac, e também solicitou a inclusão de informações sobre possíveis riscos de SGB na bula dos respectivos fabricantes.
“A Anvisa mantém a recomendação pela continuidade da vacinação com todas as vacinas contra covid-19 aprovadas pela agência, dentro das indicações descritas em bula, uma vez que, até o momento, os benefícios das vacinas superam os riscos”, indica o texto.
Dados da Anvisa registrados no Painel de Notificações de Farmacovigilância da agência até 6 de agosto de 2021 mostravam oito casos suspeitos de SGB relacionados à vacina da Janssen. Até 11 de agosto foram aplicadas 4,2 milhões de doses do imunizante no país, segundo dados do Ministério da Saúde.
Pfizer e a miocardite
É verdade que casos de miocardite (inflamação do músculo cardíaco) e de pericardite (inflamação do tecido que envolve o coração) foram relatados após a vacinação contra covid-19 com imunizantes de RNA mensageiro (mRNA), como as vacinas da Pfizer e da Moderna.
No entanto, assim como ocorre com a SGB e o imunizante Janssen, os casos são considerados raros e a análise da OMS é a de que os benefícios das vacinas de mRNA superam os riscos.
Segundo o comunicado da organização, datado de julho de 2021, um forte sinal de miocardite ou pericardite tem sido relatado com vacinas de mRNA contra covid-19 nos Estados Unidos: “De acordo com os dados do Vaers dos EUA, aproximadamente 40,6 casos de miocardite por milhão de segundas doses em homens e 4,2 casos por milhão entre mulheres foram relatados até 11 de junho de 2021 em pessoas de 12 a 29 anos que receberam as vacinas de mRNA COVID-19. Para pessoas com mais de 30 anos, as taxas de notificação foram de 2,4 e 1,0 por milhão de segundas doses, respectivamente, para homens e mulheres”.
Ainda em junho de 2021, a FDA emitiu um comunicado anunciando revisões nas fichas técnicas das vacinas Moderna e Pfizer para incluir informações sobre um maior risco de miocardite e pericardite após a vacinação.
Segundo os CDC, os casos confirmados ocorreram, em sua maior parte, em adolescentes e jovens adultos e mais frequentemente após a segunda dose.
“Desde abril de 2021, houve mais de mil notificações no Vaers de casos de inflamação no coração - miocardite e pericardite - após a vacinação com imunizantes de mRNA (Pfizer-BioNTec, Moderna) nos Estados Unidos. Estes eventos são raros, considerando as centenas de milhões de doses administradas. A maioria dos pacientes que receberam atendimento responderam bem ao tratamento e rapidamente se sentiram melhor”, acrescentaram os CDC.
Na Europa, a Agência de Medicamentos Europeia (EMA, na sigla em inglês) publicou um comunicado em julho de 2021, no qual relata uma análise de 145 casos de miocardite entre pessoas que receberam Comirnaty (Pfizer) e 19 casos após o uso do imunizante Spikevax (Moderna). A agência europeia também manteve a posição de que os benefícios superam os riscos.
Em Israel, onde a vacinação com o imunizante da Pfizer ocorreu mais rapidamente do que na maioria dos países, o Ministério da Saúde anunciou no início de junho de 2021 as conclusões de um estudo sobre um possível vínculo entre a miocardite e as vacinas contra a covid-19. Os dados mostraram 275 casos de miocardite ocorridos entre dezembro de 2020 e maio de 2021 sobre mais de cinco milhões de pessoas vacinadas.
Além disso, o ministério israelenese indicou que 95% das pessoas com miocardite "foram consideradas com casos leves".
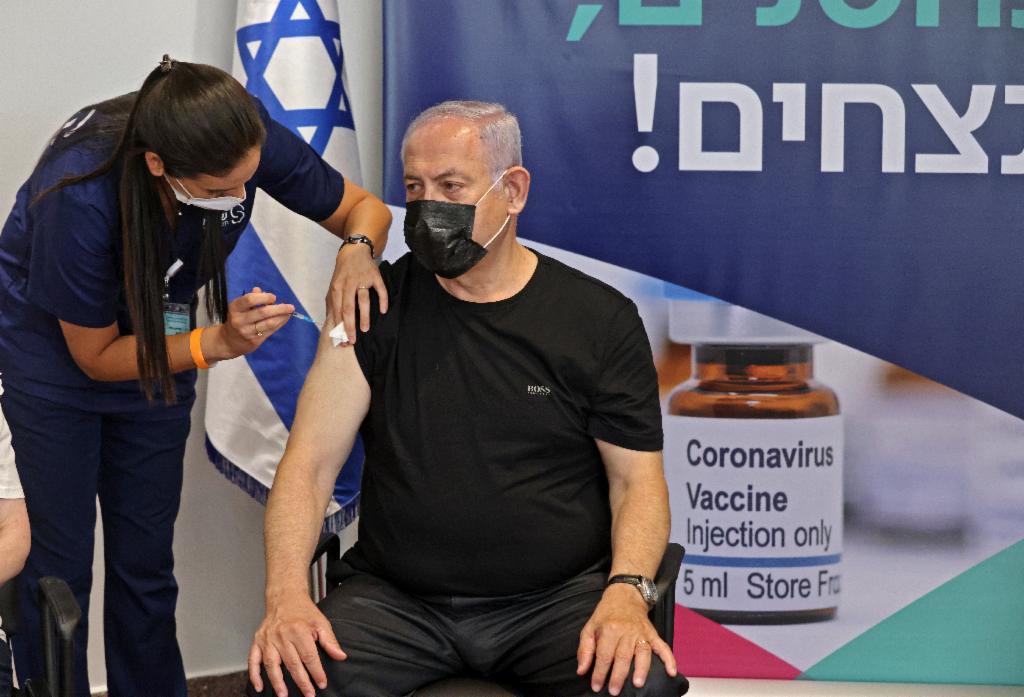
Já no Brasil, em nota publicada em 9 de julho, a Anvisa afirmou que não haviam sido registrados relatos destas complicações no Brasil. Procurada pela AFP em 9 de agosto, a agência informou que, desde a publicação da nota, quando os casos foram notificados nos EUA, foram recebidas 13 notificações de suspeitas de pericardite e miocardite, sendo quatro desta última. “Os dados não alteram a relação de benefício-risco das vacinas”, acrescentou a Anvisa.
Apesar de os casos serem raros, a agência brasileira recomenda aos profissionais de saúde que fiquem atentos e perguntem às pessoas que apresentarem sintomas se elas foram imunizadas, especialmente com a vacina da Pfizer, e orientem que procurem atendimento médico imediato se tiverem sintomas como dor no peito, falta de ar e palpitações.
AstraZeneca e a trombose
Segundo a Associação Brasileira de Hematologia, Hemoterapia e Terapia Celular (ABHH), a trombose é uma “patologia caracterizada pela formação ou desenvolvimento de um coágulo sanguíneo responsável por causar inflamação na parede do vaso, conhecida pelos médicos como trombose venal profunda”. A doença é mais comum em mulheres, e, em casos mais graves, pode levar à embolia pulmonar quando o coágulo se desloca e migra até os pulmões.
Em abril de 2021, a Agência Europeia de Medicamentos anunciou que coágulos no sangue deveriam ser listados como efeitos colaterais “muito raros” nas bulas das vacinas contra a covid-19 baseadas em vetores virais, como as da AstraZeneca e da Johnson & Johnson, destacando novamente que os benefícios dos imunizantes superam os riscos. Esse tipo de vacina usa outro vírus como suporte para transportar informações genéticas capazes de combater a covid-19.
Alguns países tomaram medidas para evitar casos excepcionais de trombose provocados pela vacinação. A Dinamarca, por exemplo, não usa os imunizantes da AstraZeneca e da Janssen, enquanto outros países como França e Holanda optaram por não aplicar AstraZeneca em grupos de determinadas idades.
No Brasil, em abril de 2021, a Anvisa solicitou a inclusão de casos raros de trombose com trombocitopenia (TTS) na bula da vacina de Oxford/AstraZeneca/Fiocruz.
O surgimento de coágulos sanguíneos importantes em combinação com níveis baixos de plaquetas no sangue (trombocitopenia) aparecem no documento como um efeito colateral “muito raro”, tendo sido observado com uma frequência inferior a um em 100.000 indivíduos vacinados.
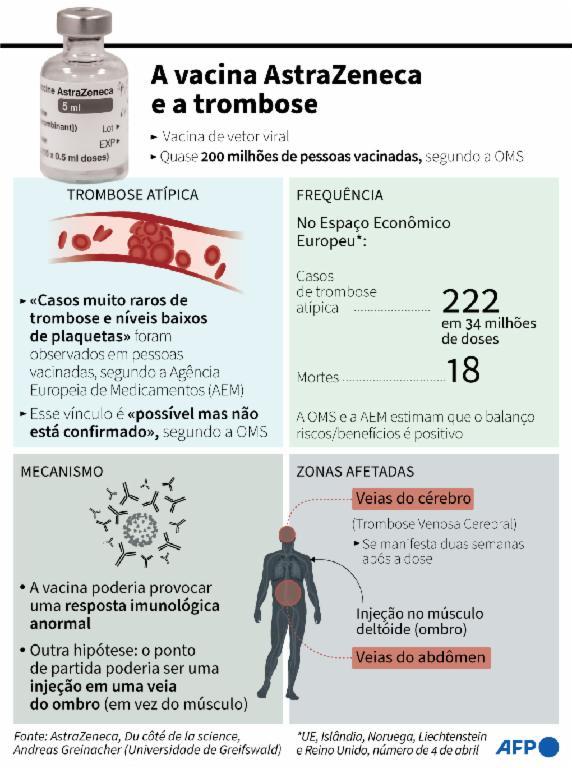
Em junho de 2021, a Anvisa emitiu um comunicado sobre casos raros de trombose após a vacinação: “Os eventos adversos mais comuns após a vacinação são dor no local da aplicação, dor de cabeça e febre. A maioria dos efeitos colaterais que ocorre com o uso das vacinas é de natureza leve e transitória, não permanecendo por mais que 72 horas. O risco de ocorrência de coágulos sanguíneos é baixíssimo, mas o cidadão deve estar atento aos possíveis sintomas associados à TTS”.
A Anvisa ressaltou, ainda, que mantém a recomendação pela continuidade da vacinação com o imunizante, uma vez que, até o momento, os benefícios superam os riscos associados à infecção por covid-19.
Segundo o Painel de Vigilância de Efeitos Adversos da Anvisa, até 4 de agosto de 2021, foram registradas 139 notificações de suspeitas de trombose associadas ao uso da vacina AstraZeneca.
Até 11 de agosto de 2021 já foram aplicadas 70,89 milhões de doses da vacina Astrazeneca no Brasil, segundo dados do Ministério da Saúde. Isso significa que as notificações de suspeitas de trombose equivalem a 0,000196% do total de doses aplicadas.
CoronaVac e o risco de contrair covid-19
O imunizante CoronaVac é produzido no Brasil pela farmacêutica Sinovac em parceria com o Instituto Butantan. Em seu site, o instituto explica que a vacina utiliza a tecnologia de vírus inativado, uma técnica já consolidada na produção de vacinas. “Ao ser injetado no organismo, esse vírus não é capaz de causar doença, mas induz uma resposta imunológica”, diz a instituição.
Em junho de 2021, a OMS aprovou o uso emergencial da CoronaVac, relatando uma eficácia observada de 51% em prevenir infecções sintomáticas. Além disso, a OMS concluiu que a CoronaVac preveniu a covid-19 grave e hospitalização em 100% da população estudada.
Em julho, a Fiocruz, instituição de pesquisa científica responsável pela produção da vacina AstraZeneca no Brasil, concluiu que a CoronaVac manteve sua eficácia em idosos mesmo frente à variante P.1. A fundação concluiu que, entre os vacinados com as duas doses da CoronaVac, os índices de efetividade foram de 79,6% de 60 a 79 anos, e 68,8% acima dos 80 anos.
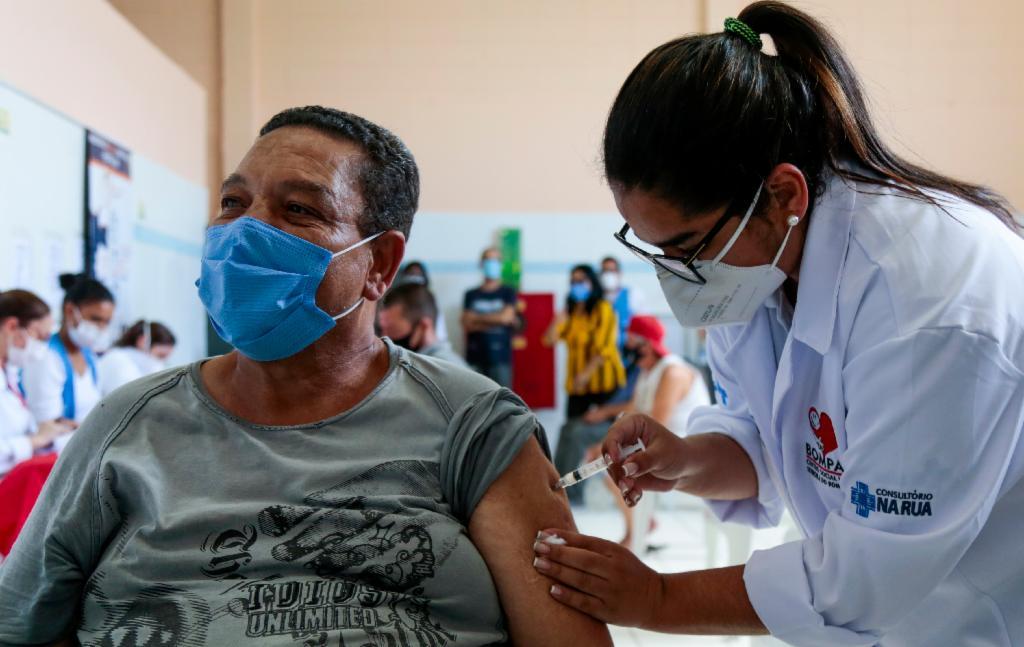
Um estudo publicado em julho de 2021 na revista científica New England Journal of Medicine a respeito do uso da CoronaVac no Chile concluiu que a vacina teve uma efetividade de 65,9% na prevenção da covid-19 sintomática; 87,5% na prevenção de hospitalização; 90,3% na prevenção de entrada em UTIs e 86,3% na prevenção de mortes por covid-19. O estudo analisou a campanha de vacinação do Chile entre 2 de fevereiro e 1º de maio de 2021, que incluiu 10,2 milhões de chilenos.
Outro estudo divulgado pelo Ministério da Saúde do Chile em agosto concluiu que a CoronaVac teve 58,49% de eficácia para prevenir a covid-19 sintomática; 86,02% de efetividade para prevenir hospitalização; 89,68% para prevenir ingresso em UTI e 86,38% para prevenir mortes por covid-19.
Em 5 de agosto, o Chile anunciou que aplicaria uma dose de reforço usando os imunizantes AstraZeneca e Pfizer, considerando “a evolução da efetividade com o tempo das vacinas e o risco da variante Delta”, segundo o presidente Sebastián Piñera. Decisão similar foi tomada no Uruguai, que também utilizou a CoronaVac em grande escala.
Desde que a vacina foi aprovada para uso emergencial no Brasil, a AFP já verificou diversas alegações sobre a suposta ineficácia da CoronaVac (1, 2, 3).
Copyright © AFP 2017-2026. Qualquer uso comercial deste conteúdo requer uma assinatura. Clique aqui para saber mais.